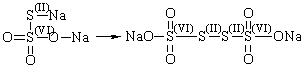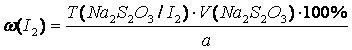|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Препараты
VIIA группы
периодической системы
|
|
|
Йод Натрия хлорид Калия хлорид Натрия бромид Калия бромид Натрия йодид Калия йодид |
Iodum – Йод
I2 М.м.
253,8 Описание. Серовато-черные с
металлическим блеском пластинки или сростки кристаллов характерного запаха.
Летуч при обыкновенной температуре, при нагревании возгоняется, образуя
фиолетовые пары. Получение. Источники: 1.
Буровые воды нефтяных скважин, 2.
Зола морских водорослей, 3.
Селитроносные породы. Угольно-адсорбционный метод получения йода из буровых вод
нефтяных скважин. Этапы: 1.
Очистка нефтяных вод от нафтеновых кислот подкислением, 2.
Фильтрация, 3.
Окисление йодидов нитритом натрия до свободного йода: 2NaI + 2NaNO2 + 2H2SO4 → I2 + 2NO↑ + 2Na2SO4 +
2H2O, 4.
Адсорбция йода в колонках с активированным углем (концентрирование йода
увеличивается в 200–300 раз), 5.
Десорбция йода с помощью восстановителей: I2 + Na2SO3 + H2O → 2HI + Na2SO4, 6.
Фильтрация, 7.
Окисление до йода хлором, хлоратом калия или электролизом: 2NaI + Cl2 → I2 + 2NaCl, 8.
Очистка йода сублимацией. Растворимость. Очень мало растворим в
воде, легко растворим в водном растворе йодидов, растворим в 10 ч. 95%
спирта, в эфире и хлороформе. Растворы в хлороформе фиолетового цвета. Подлинность. 1.
Реакция с крахмалом (ГФ Х) с образованием фиолетового
окрашивания; при нагревании окрашивание исчезает, при охлаждении – появляется
вновь. Прозрачность
и цветность раствора. Растворение препарата в водном растворе тиосульфата натрия, образуя
прозрачный и бесцветный раствор: I2 + 2Na2S2O3 → 2NaI + Na2S4O6.
Йодистый
циан.
Образуется при получении йода из золы морских водорослей: I2 + 2C + N2 → 2ICN. Препарат растирают с водой и фильтруют; 1/3
фильтрата обесцвечивают раствором сернистой кислоты: I2 + H2SO3 + H2O → H2SO4 + 2HI, Добавляют растворы хлорида
железа (III) и гидроксида натрия; смесь нагревают и
подкисляют разведенной соляной кислотой. Не должно появляться
сине-фиолетового окрашивания (образование берлинской лазури): ICN + 2NaOH → NaCN + NaIO + H2O; 2NaCN + FeSO4 → Fe(CN)2 + Na2SO4, Fe(CN)2 + 4NaCN → Na4[Fe(CN)6], Na4[Fe(CN)6] + FeCl3 → NaFe[Fe(CN)6]↓ + 3NaCl. Галогениды. Остальные 2/3 фильтрата
обесцвечивают раствором сернистой кислоты, добавляют концентрированный
раствор аммиака, осаждают иодиды раствором нитрата серебра, фильтруют;
фильтрат подкисляют и определяют хлориды и бромиды: [Ag(NH3)]Cl +HNO3 → AgCl↓ + NH4NO3, [Ag(NH3)]Br +HNO3 → AgBr↓ + NH4NO3. Образующееся помутнение сравнивают с эталоном. Количественное
определение. Прямое титрование (ГФ Х). Титрант
– Na2S2O3, индикатор – крахмал. I2 + 2Na2S2O3 → 2NaI + Na2S4O6. fэкв(I2)=1/2, Хранение. Список Б. В стеклянных банках с притертыми пробками, в
прохладном, защищенном от света месте. Применение. Антисептик. Solutio Iodi spirituosa (5%) – Раствор Йода спиртовой (5%)
Tinctura Iodi 5% – Настойка йодная (5%) Состав. Йода Калия
йодида Воды
и спирта 95% поровну до Описание. Прозрачная жидкость
красно-бурого цвета с характерным запахом. Подлинность. Реакция с крахмалом. Спирт не менее 46%. Количественное
определение. 1.
Прямое титрование. Титрование навески
препарата тиосульфатом натрия без индикатора до обесцвечивания раствора: I2 + 2Na2S2O3 → 2NaI + Na2S4O6, fэкв(I2)=1/2, Титрование по методу
Фаянса. К оттитрованной жидкости добавляют разведенную уксусную кислоту и
индикатор (роданид натрия): K[I3] + 2Na2S2O3 → KI + 2NaI + Na2S4O6, KI + AgNO3 2NaI + 2AgNO3 fэкв(KI)=1, Хранение. Список Б. В стеклянных банках оранжевого стекла, в прохладном,
защищенном от света месте. Solutio Iodi spirituosa (10%) – Раствор Йода спиртовой (10%)
Tinctura Iodi 10% – Настойка йодная (10%) Состав. Йода Спирта
95% до Описание. Жидкость красно-бурого цвета
с характерным запахом. Подлинность. При разбавлении препарата
водой выпадают кристаллы йода. |
|
|
|
|
|